發(fā)布時間:2022年2月17日 作者:“德國GMCI高美測儀”關注我們!
支持醫(yī)療器械we一標識(UDI)的醫(yī)療電氣安規(guī)測試儀

UDI定義
醫(yī)療器械we一標識(Unique Device Identification,縮寫UDI)是對醫(yī)療器械在其整個生命周期賦予的身份標識,是其在產品供應鏈中的we一“身份證”。全球采用統(tǒng)一的、標準的UDI有利于提高供應鏈透明度和運作效率;有利于降低運營成本;有利于實現(xiàn)信息共享與交換;有利于不良事件的監(jiān)控和問題產品召回,提高醫(yī)療服務質量,保障患者安全。
UDI組成
01) DI(Device Identifier)產品標識(或器械識別碼)
產品標識(或器械識別碼)是UDI 的固定和強制性部分,它包含貼標者(labeler)信息和產品型號。產品標識是識別醫(yī)療器械注冊人或者備案人、醫(yī)療器械型號規(guī)格和包裝的we一碼。
02) PI(Production Identifier) 生產標識(或生產識別碼)
生產標識(或生產識別碼)是UDI 的可變和非強制性部分,根據監(jiān)管和實際應用需求可包含醫(yī)療器械序列號、生產批號、生產日期、失效日期等。生產標識是識別醫(yī)療器械生產過程相關數據的代碼。
UDI世界各國的進展
根據歐洲醫(yī)療器械行業(yè)協(xié)會介紹,國際醫(yī)療器械監(jiān)管機構論壇(原GHTF)從2011年提出的D一版的UDI系統(tǒng)指導文件開始,UDI已經不再是美國d有的醫(yī)療器械w一識別碼,而成為世界范圍的醫(yī)療器械規(guī)范的識別碼(globally harmonized UDI system)。
醫(yī)療器械w一標識,并不是醫(yī)療器械行業(yè)近幾年新誕生的要求,而在ISO 13485體系中本身就有可追溯性要求的要素,但從行業(yè)發(fā)展的觀點看,UDI是全球性的醫(yī)療器械w一標識系統(tǒng),也是全球醫(yī)療器械市場國際化發(fā)展的必然趨勢。
2017年2月《國務院關于印發(fā)“十三五”國家食品安全規(guī)劃和“十三五”國家藥品安全規(guī)劃的通知》提出,制定醫(yī)療器械編碼規(guī)則,構建醫(yī)療器械編碼體系。
藥品監(jiān)管局和行業(yè)聯(lián)盟正積極參與國內相關法規(guī)、標準的轉化和制定工作,推出了標準化電子貨單、公共主數據、首營交換平臺、全程追溯及監(jiān)管平臺等服務產品。另外,越來越多出口企業(yè)由于生產發(fā)展及供應鏈管理需求,開始自主實施UDI。
醫(yī)療電氣安規(guī)測試儀如何支持UDI及新標準?
針對醫(yī)療器械的研發(fā)、生產和售后維修服務,有一系列強制的電氣安全標準,醫(yī)療電氣設備常用的測試標準有IEC60601-1(醫(yī)療電氣設備的安全測試)和IEC62353(醫(yī)療電氣設備的循環(huán)試驗和維修后試驗)。
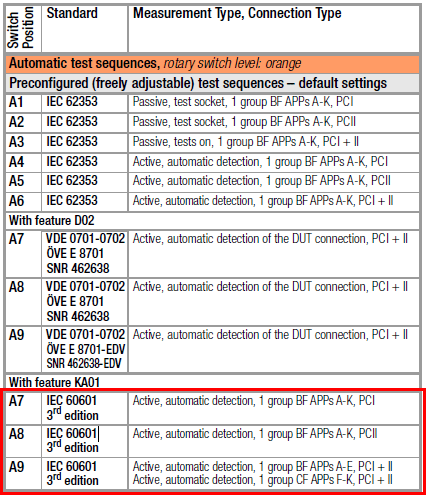
目前IEC60601新的第三版標準,針對測試方法和限值都有變化:

德國GMC-I新款醫(yī)療電氣安規(guī)測試儀SECULIFE ST PRO預設9個自動測試序列,已經包含IEC60601第三版的測試序列;而且用戶還可根據實際需求自定義修改測試序列。

德國GMC-I新款醫(yī)療電氣安規(guī)測試儀SECULIFE ST PRO可全面醫(yī)療器械w一標識UDI(Unique Device Identification)。測試儀器數據管理系統(tǒng)有專門的醫(yī)療設備(ME equipment **)信息錄入目錄,可錄入被測醫(yī)療器械的UDI。
